<rp id="mbqar"></rp> <ol id="mbqar"><optgroup id="mbqar"></optgroup></ol> NEWS
新聞資訊
科研合作
01.前言
低級(jí)別漿液性卵巢癌(LGSOC)是一種較為少見的卵巢上皮癌(EOC),約占全部卵巢癌的5%。LGSOC與高級(jí)別漿液性卵巢癌(HGSOC)的分子通路、生物學(xué)行為、臨床特征不同。LGSOC多見于年輕女性,中位發(fā)病年齡43歲,較HGSOC發(fā)病年輕10歲。其生長(zhǎng)緩慢,腫瘤呈惰性,且對(duì)以鉑類為基礎(chǔ)的化療相對(duì)不敏感。雖然與HGSOC相比預(yù)后較好,但I(xiàn)II/IV期腫瘤的長(zhǎng)期生存數(shù)據(jù)仍不理想。LGSOC通常繼發(fā)于漿液性交界性腫瘤(SBOT),常見BRAF和KRAS基因突變。高分期腫瘤中少見BRAF突變,KRAS突變可能是LGSOC進(jìn)展的驅(qū)動(dòng)因素。絲裂原活化蛋白激酶(MAPK)通路在LGSOC發(fā)生、發(fā)展中發(fā)揮重要作用,靶向該通路的療法在LGSOC的治療中顯得尤為關(guān)鍵[1-3]。
02.LGSOC的分子機(jī)制
LGSOC通常繼發(fā)于SBOT,LGSOC的組織形態(tài)、分子通路與SBOT的相關(guān)度達(dá)到75%以上。SBOT經(jīng)過一系列的基因突變進(jìn)展成為L(zhǎng)GSOC,其中包括BRAF、KRAS和ERBB2基因,最終導(dǎo)致MAPK通路持續(xù)活化[3]。LGSOC經(jīng)常攜帶KRAS(19%~55%)和BRAF(0~33%,平均5%)基因突變,也可能存在NRAS、USP9X和EIF1AX突變,染色體9p缺失或CDKN2A/2B雜合性缺失。BRAF基因在LGSOC中的突變頻率低于SBOT(5% vs 23%-48%),且BRAF突變患者預(yù)后更好,提示BRAF可能為保護(hù)性基因。KRAS基因突變可能是LGSOC進(jìn)展驅(qū)動(dòng)因素,與腫瘤復(fù)發(fā)有關(guān)[2-3]。此外,NRAS突變僅限于浸潤(rùn)性癌癥中,NRAS突變患者年齡大、晚期疾病比例更高,殘留病灶更多[4]。除了基因突變外,MAPK通路基因的缺失和融合可能也與MEK抑制劑療效相關(guān);部分LGSOC患者也可能存在PI3K等通路活化[3]。
Dane Cheasley等研究者分析了來自全外顯子組(WES)測(cè)序隊(duì)列的71例LGSOC患者的127個(gè)候選基因,以生成突變和拷貝數(shù)變異數(shù)據(jù);并進(jìn)行了免疫組織化學(xué)(IHC)檢測(cè),評(píng)估了雌激素受體(ER)、孕激素受體(PR)、p53和CDKN2A狀態(tài)。靶向測(cè)序發(fā)現(xiàn)47%的病例存在MAPK通路基因(KRAS(26.7%)、BRAF(12.6%)和NRAS(8.5%))突變,以及USP9X(27%)、MACF1(11%)、ARID1A(9%)等驅(qū)動(dòng)基因突變。IHC顯示常見ER/PR陽(yáng)性(85%),CDKN2A蛋白丟失(10%)或過表達(dá)(6%),所有樣本均為p53野生型。與HGSOC不同,LGSOC的同源重組修復(fù)缺陷(HRD)評(píng)分平均僅為3(0-48)分,僅有3例評(píng)分大于42分被判為陽(yáng)性[5]。
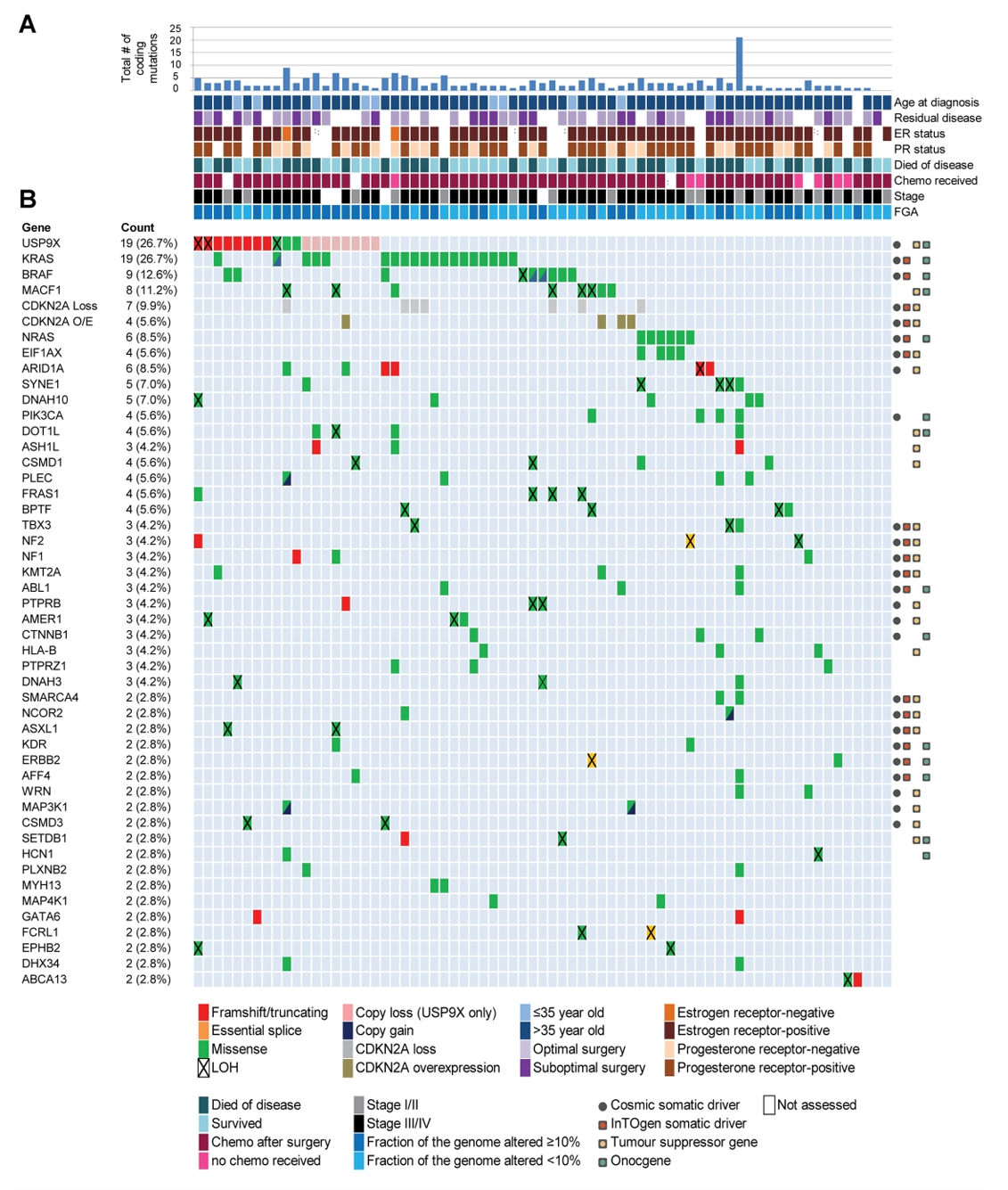
LGSOC隊(duì)列突變譜[5]
David M Gershenson等研究者報(bào)道了一項(xiàng)LGSOC隊(duì)列MAPK通路突變特征研究結(jié)果:共納入接受了高通量測(cè)序(NGS)檢測(cè)的215例LGSOC患者,診斷時(shí)的中位年齡為46.6歲,大多數(shù)為III期原發(fā)性卵巢癌。140例(65.1%)的病例中發(fā)現(xiàn)一個(gè)或多個(gè)突變,52.6%的患者在MAPK通路中發(fā)生突變,突變基因包括KRAS、NRAS、BRAF、MAP2K1和RAF1,最常見的突變是KRAS(n=71,33.0%)、NRAS(n=24,11.2%)和BRAF(n=18,8.4%)。71個(gè)KRAS突變包括33個(gè)G12D、29個(gè)G12V、3個(gè)G12A、2個(gè)G12R、1個(gè)G12S、G12C和G12_G13insAG。MAPK通路突變患者的無進(jìn)展生存(PFS)數(shù)據(jù)優(yōu)于未檢出MAPK突變的患者(31.4個(gè)月 vs 23.7個(gè)月,p=0.002)。MAPK通路突變患者的總生存(OS)數(shù)據(jù)優(yōu)于未檢出MAPK突變的患者(147.8個(gè)月 vs 89.5個(gè)月,p=0.01),亦優(yōu)于腫瘤未檢出突變的患者(147.8個(gè)月 vs 78個(gè)月,p=0.001)[6]。
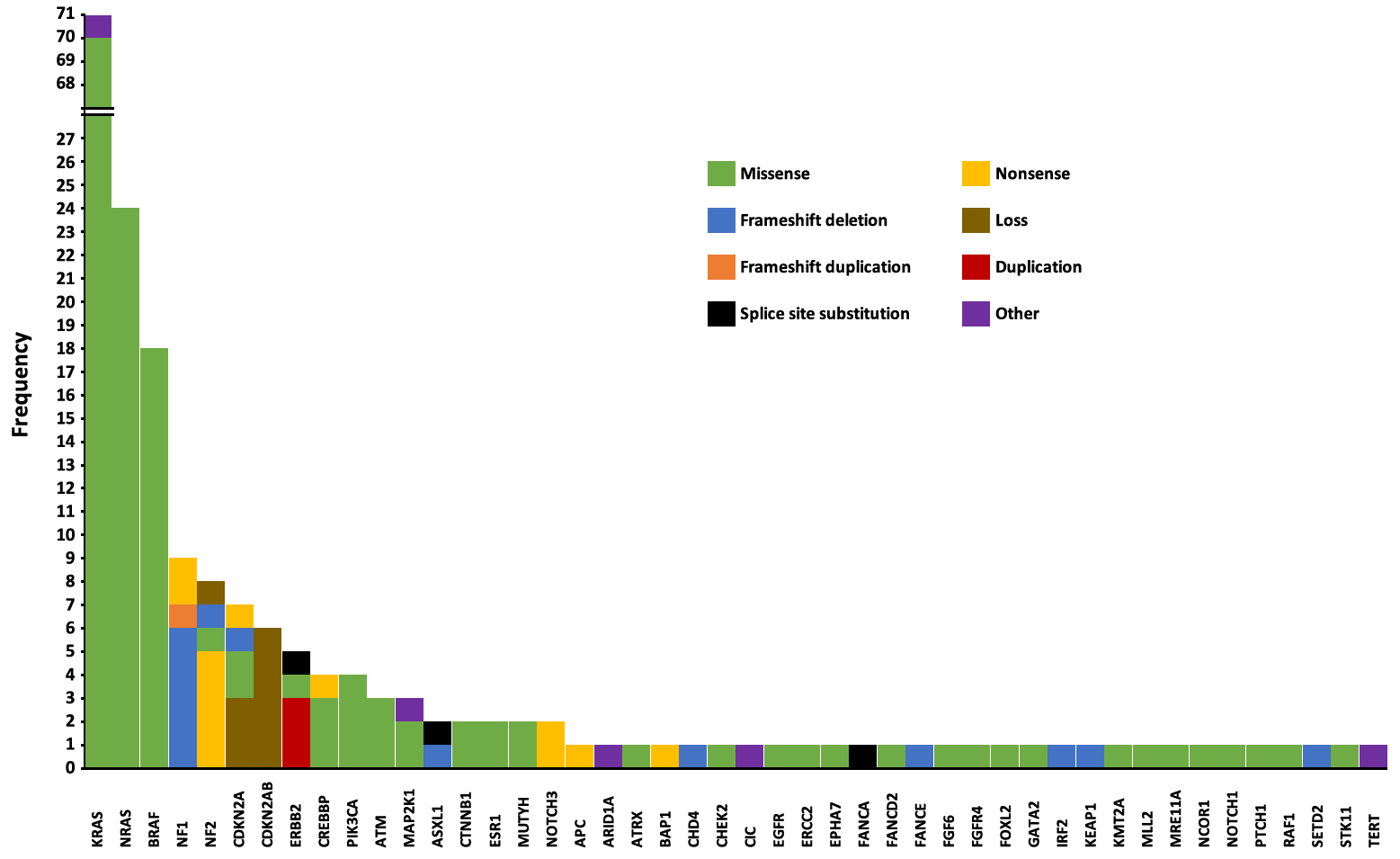
215例LGSOC患者的基因突變頻率[6]
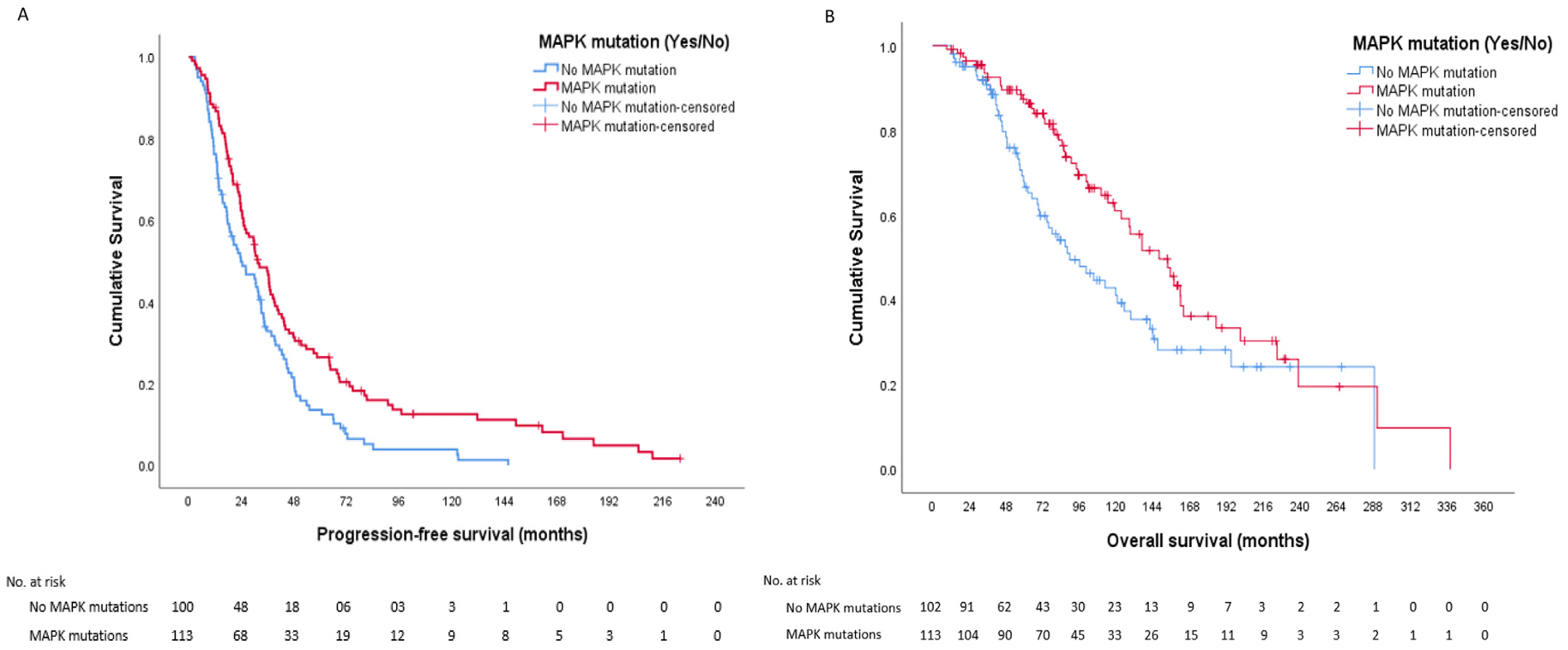
MAPK突變患者與未檢出MAPK突變患者的PFS和OS比較[6]
03. LGSOC的靶向療法
一直以來,NCCN對(duì)復(fù)發(fā)性LGSOC系統(tǒng)治療的推薦主要為BRAF/MEK抑制劑:曲美替尼(2A類證據(jù))、Binimetinib(2B類證據(jù))、達(dá)拉非尼聯(lián)合曲美替尼(BRAF V600E陽(yáng)性腫瘤,2A類證據(jù))[7]。
GOG-0281研究(NCT02101788)比較了MEK抑制劑曲美替尼與標(biāo)準(zhǔn)治療組治療復(fù)發(fā)性LGSOC的效果,共納入260例患者,隨機(jī)1:1分配,主要終點(diǎn)為研究者評(píng)估的PFS。兩個(gè)亞組均有約一半的患者進(jìn)行了WES測(cè)序,17%的患者檢測(cè)到KRAS、BRAF或NRAS突變。與標(biāo)準(zhǔn)治療組比較,曲美替尼顯著延長(zhǎng)了復(fù)發(fā)性LGSOC患者的中位PFS(13.0個(gè)月vs 7.2個(gè)月,風(fēng)險(xiǎn)比(HR)=0.48,P<0.0001)。客觀緩解率(ORR)為26%比6%(優(yōu)勢(shì)比(OR)=5.4,P<0.0001),另有59%的患者疾病穩(wěn)定至少8周。持續(xù)緩解時(shí)間(DOR)延長(zhǎng)(13.6個(gè)月vs 5.9個(gè)月)。中位OS為37.6個(gè)月vs 29.2個(gè)月(HR=0.76,P=0.056),有利于曲美替尼組。RAS/BRAF突變患者的PFS和ORR均優(yōu)于野生型患者,但無統(tǒng)計(jì)學(xué)差異[8]。
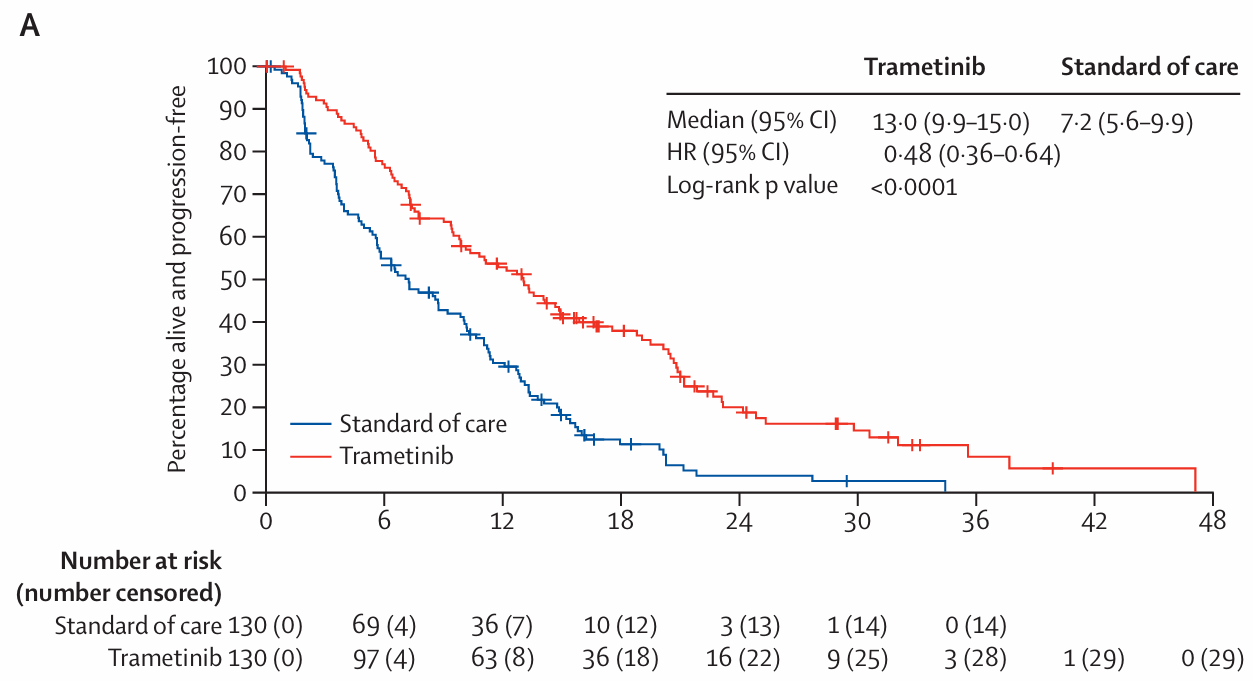
意向治療人群PFS的KM分析[8]
MILO/ENGOT-ov11研究(NCT01849874)招募了341例復(fù)發(fā)性LGSOC患者,以2:1隨機(jī)分配至Binimetinib組或醫(yī)師選擇的化療(PCC)組,主要終點(diǎn)為盲態(tài)獨(dú)立評(píng)審委員會(huì)(BICR)評(píng)估的PFS。303例患者的中期分析發(fā)現(xiàn),Binimetinib組對(duì)比PCC組,中位PFS為9.1個(gè)月vs 10.6個(gè)月(HR=1.21,p=0.807),根據(jù)預(yù)先設(shè)定的無效邊界提前結(jié)束研究。215例接受了分子檢測(cè),33%檢出KRAS突變。Binimetinib組中,KRAS突變與野生型患者相比,應(yīng)答率為44% vs 19%(p=0.004),中位PFS為17.7個(gè)月 vs 10.8個(gè)月(p=0.006),而PCC組的PFS則沒有這種關(guān)聯(lián)(p=0.502)。其他檢測(cè)到的MAPK通路改變包括NRAS(n=11,8.1%)、BRAF V600E(n=8,5.9%)、RAF1(n=2,1.5%)和NF1(n=7,5.2%)。Binimetinib組中,MAPK變異與野生型患者相比,應(yīng)答率為41% vs 13%(p<0.001),且有更長(zhǎng)的PFS(HR=0.5,p=0.003)[9-10]。

Binimetinib組和PCC組PFS的KM分析:A、KRAS突變,B、MAPK變異[10]
2022年6月22日,美國(guó)食品藥品監(jiān)督總局(FDA)批準(zhǔn)BRAF抑制劑達(dá)拉非尼聯(lián)合曲美替尼用于BRAF V600E突變的不可切除或轉(zhuǎn)移性實(shí)體瘤患者的后線治療。這一獲批基于多項(xiàng)臨床試驗(yàn)結(jié)果,其中一項(xiàng)為NCI-MATCH試驗(yàn)(NCT02465060)H亞組(EAY131-H)。研究納入了6例婦科腫瘤患者,其中5例為L(zhǎng)GSOC,ORR達(dá)到了80%[11]。研究的總體中位PFS為11.4個(gè)月,中位OS為28.6個(gè)月[12]。
在HGSOC中應(yīng)用廣泛的PARP抑制劑,在臨床試驗(yàn)的入組標(biāo)準(zhǔn)中清一色地沒有納入LGSOC患者[13]。前述中也提到LGSOC的分子機(jī)制與HGSOC不同,HRD評(píng)分一般較低,所以目前沒有臨床研究數(shù)據(jù)支持LGSOC患者使用PARP抑制劑的療效。
04. KRAS突變LGSOC的新療法
2025年5月8日,F(xiàn)DA加速批準(zhǔn)了VERASTEM INC的Avutometinib 聯(lián)合Defactinib(AVMAPKI FAKZYNJA CO-PACK)用于至少接受過一次系統(tǒng)治療的、KRAS突變的復(fù)發(fā)性LGSOC成人患者。這是LGSOC獲批的首個(gè)KRAS靶向療法。Avutometinib(VS-6766)是一種RAF/MEK鉗夾,可以誘導(dǎo)無活性RAF/MEK復(fù)合物的形成,抑制RAF磷酸化MEK1/2。Defactinib是粘著斑激酶(FAK)和富含脯氨酸的酪氨酸激酶2(Pyk2)的選擇性抑制劑, 可以抑制FAK的自磷酸化。Avutometinib聯(lián)合Defactinib增強(qiáng)了抑制體外細(xì)胞增殖的能力,以及包括LGSOC在內(nèi)的小鼠腫瘤模型中的抗腫瘤活性[11]。
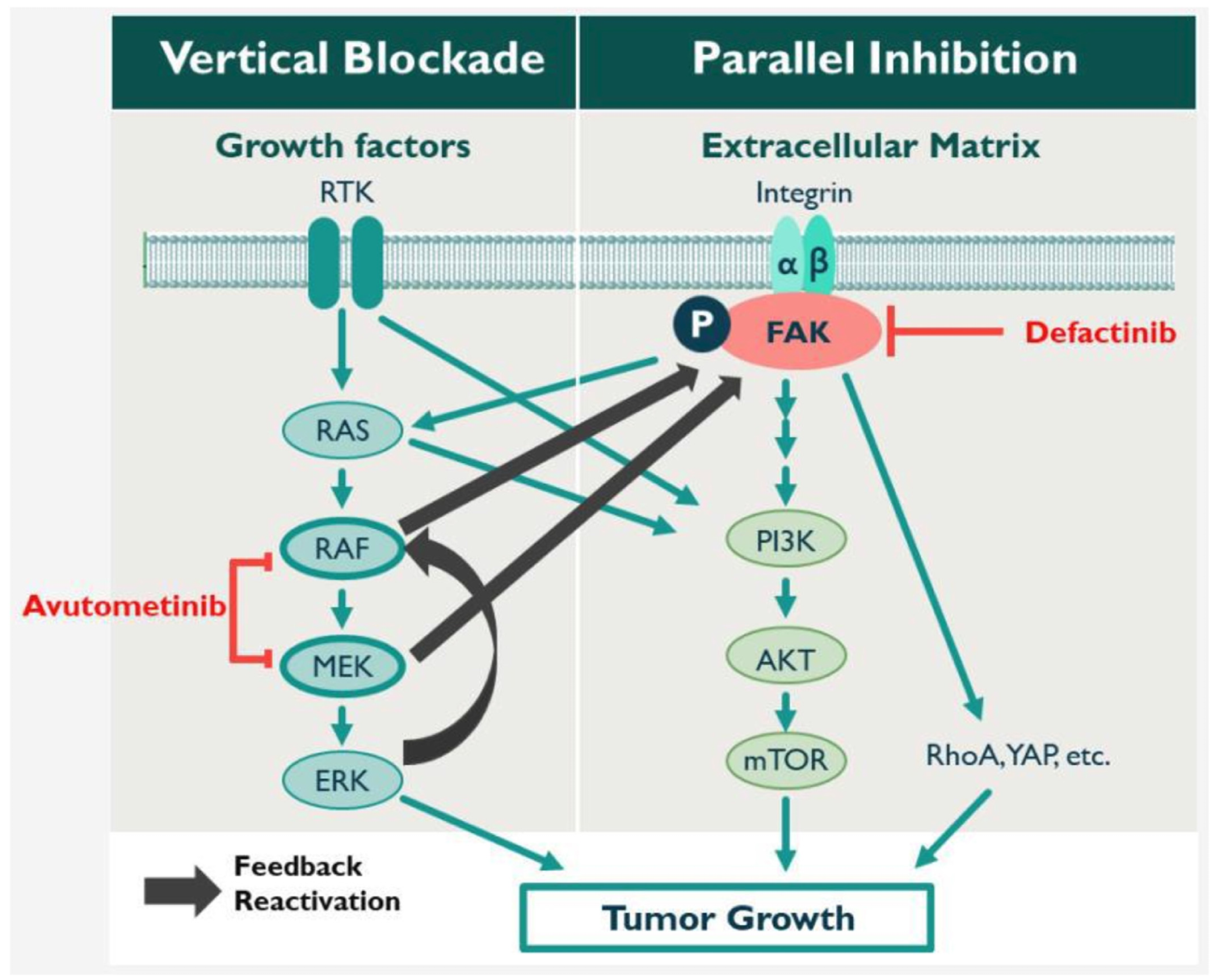
Avutometinib聯(lián)合Defactinib的作用機(jī)制[14]
其獲批基于開放標(biāo)簽的多中心II期RAMP-201 研究(NCT04625270),共納入57例KRAS突變復(fù)發(fā)性LGSOC成年患者,患者必須至少接受過一次系統(tǒng)治療,包括以鉑為基礎(chǔ)的治療方案。通過對(duì)腫瘤組織進(jìn)NGS或聚合酶鏈反應(yīng)(PCR)檢測(cè)來確定KRAS突變狀態(tài), 本次FDA并未同步批準(zhǔn)KRAS伴隨診斷檢測(cè)。患者口服Avutometinib 3.2 mg,每周2次,口服Defactinib 200 mg,每天2次,直至疾病進(jìn)展或不可耐受的毒性。研究的主要終點(diǎn)為BICR評(píng)估的ORR[11]。
鑒定出的KRAS突變包括G12V(53%)、G12D(35%)、Q61H(3.5%)、G12C(1.8%)、G12R(1.8%)、A146V(1.8%)等。57例患者的ORR為44%,其中兩例完全緩解(CR),DOR范圍從3.3至31.1個(gè)月。25例應(yīng)答患者的KRAS突變包括A146V、G12D、G12R、G12V和Q61H[11]。KRAS野生型患者的ORR為17%。KRAS突變型與野生型患者相比,中位DOR為31.1個(gè)月 vs 9.2個(gè)月,中位PFS為22個(gè)月 vs 12.8個(gè)月,6個(gè)月以上的疾病控制率(DCR)為70% vs 50%[15]。
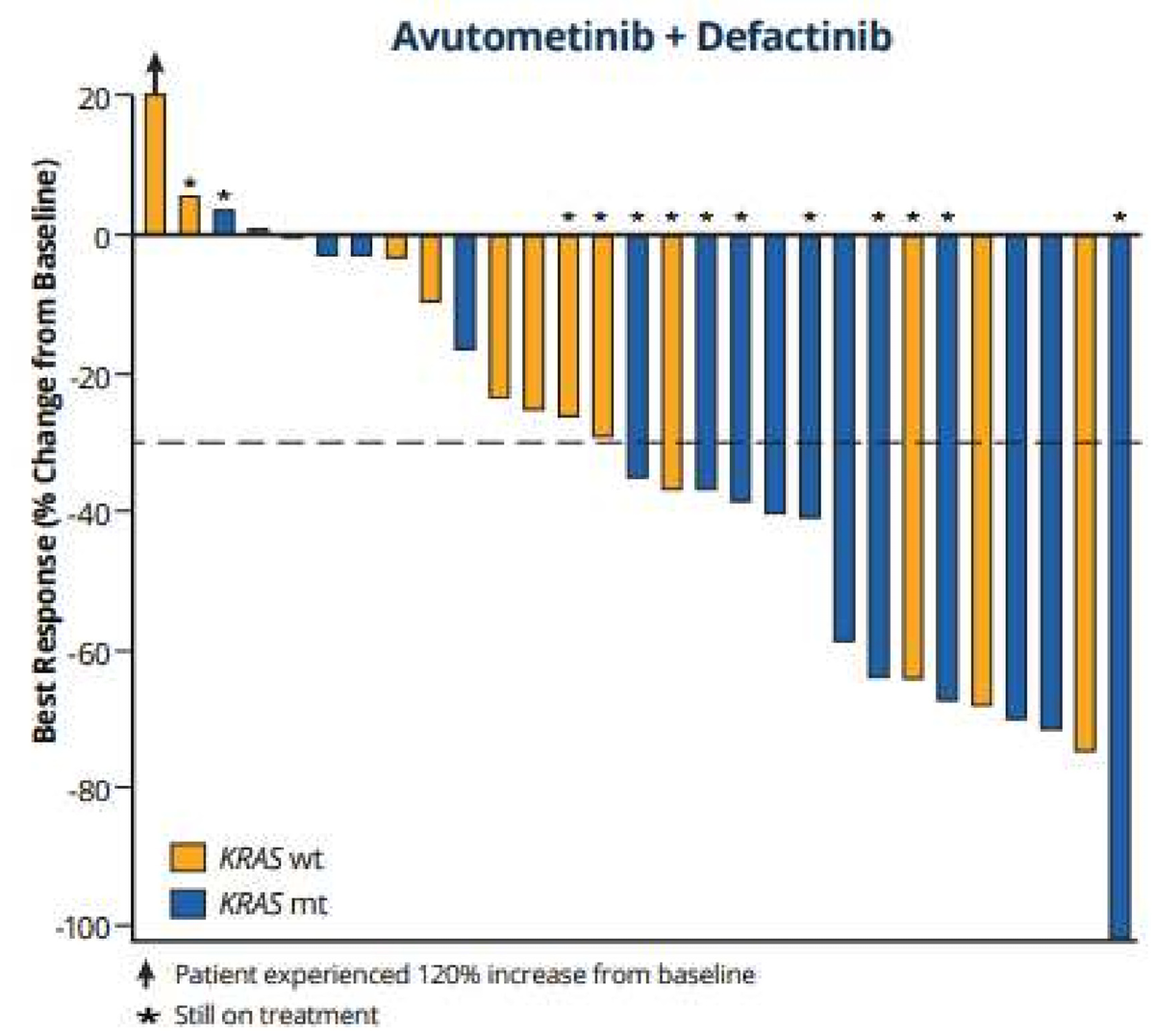
RAMP-201(PART A)的腫瘤療效評(píng)估[14]
Avutometinib聯(lián)合Defactinib治療復(fù)發(fā)性LGSOC的隨機(jī)、開放標(biāo)簽的國(guó)際多中心III期RAMP-301研究(NCT06072781)正在進(jìn)行中,大約270例患者以1:1隨機(jī)分配到Avutometinib與Defactinib聯(lián)合治療組或研究者選擇的治療組。患者必須患有復(fù)發(fā)性LGSOC(KRAS突變型或野生型),并且在至少一種鉑類化療方案后進(jìn)展或復(fù)發(fā),不限治療線數(shù),不限是否使用過MEK/RAF抑制劑。但排除HGSOC或混合組織學(xué)患者,以及接受過Avutometinib、Defactinib或其他FAK抑制劑治療的患者。主要終點(diǎn)為根據(jù)RECIST 1.1版標(biāo)準(zhǔn),BICR評(píng)估的PFS。RAMP-301 預(yù)計(jì)的主要完成日期為2028年10月15日,預(yù)計(jì)研究完成日期為2031年2月9日[13-14]。
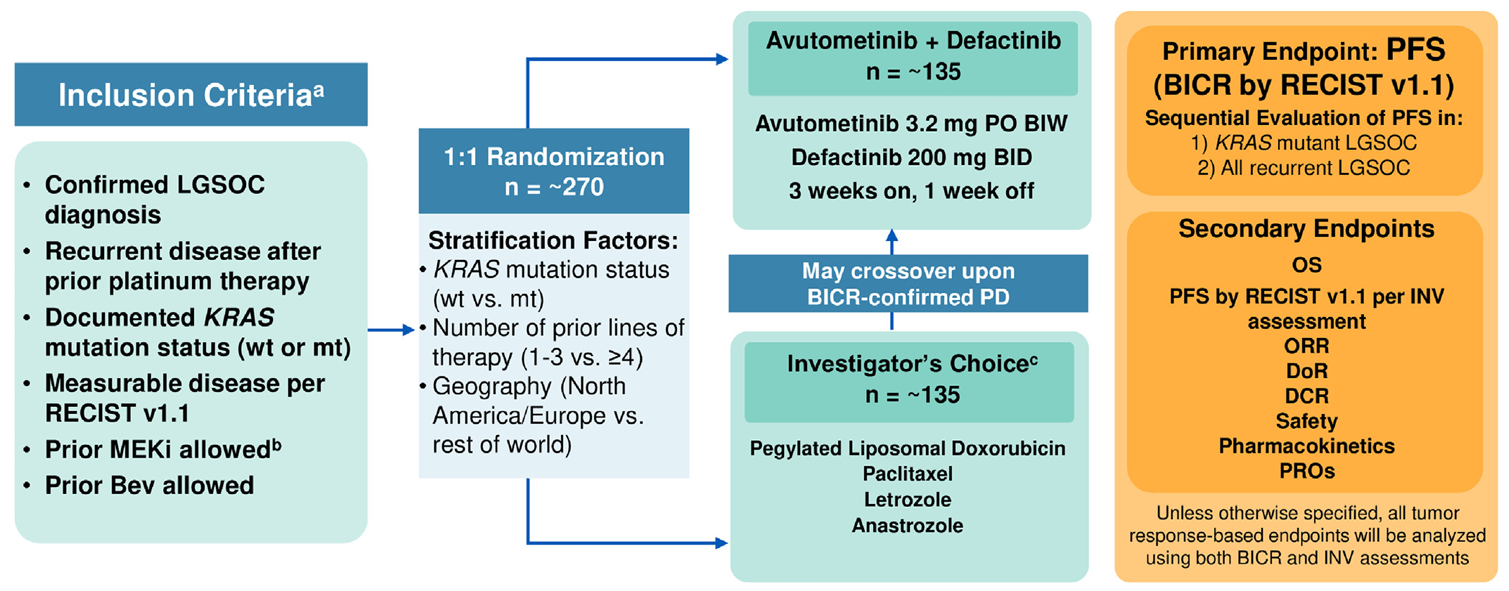
RAMP-301 研究方案[14]
05. 總結(jié)
除LGSOC之外,Avutometinib聯(lián)合Defactinib治療KRAS突變的非小細(xì)胞肺癌、胰腺癌、子宮內(nèi)膜癌、黑色素瘤等癌種的研究亦在進(jìn)行中。飛朔生物具有已獲得國(guó)家藥監(jiān)局III類醫(yī)療器械注冊(cè)證的人類K-ras基因突變檢測(cè)試劑盒(多重?zé)晒釶CR法,國(guó)械注準(zhǔn)20223400275),亦有數(shù)十個(gè)含有KRAS基因的檢測(cè)項(xiàng)目。飛朔致力于為腫瘤個(gè)體化精準(zhǔn)醫(yī)學(xué)檢測(cè)提供最具創(chuàng)新性的產(chǎn)品和服務(wù),并持續(xù)更新現(xiàn)有產(chǎn)品。
參考文獻(xiàn)
[1] 第5版WHO女性生殖系統(tǒng)腫瘤分類
[2] CSCO卵巢癌診療指南2024
[3] 低級(jí)別漿液性卵巢癌的專家共識(shí)(2020年版)
[4] Clin Cancer Res. 2014 Dec 15;20(24):6618-30.
[5] J Pathol. 2021 Jan;253(1):41-54.
[6] Gynecol Oncol. 2022 Jun;165(3):560-567.
[7] NCCN卵巢癌包括輸卵管癌和原發(fā)性腹膜癌診療指南2025 v2
[8] Lancet. 2022 Feb 5;399(10324):541-553.
[9] J Clin Oncol. 2020 Nov 10;38(32):3753-3762.
[10] Clin Cancer Res. 2023 Oct 13;29(20):4068-4075.
[11] FDA官網(wǎng)數(shù)據(jù)
[12] J Clin Oncol. 2020 Nov 20;38(33):3895-3904.
[13] Clinical Trails官網(wǎng)數(shù)據(jù)
[14] Int J Gynecol Cancer. 2025 Jan 6:ijgc-2024-005919.
[15] Verastem Oncology在IGCS 2024年年會(huì)上呈報(bào)的更新數(shù)據(jù)